
Dans ce cours, lorsque deux carbones sont liés, c'est par une liaison simple : C─ C. Pas de liaisons C=C, ni C≡C.
Autant dire que nous n'aurons ici que des chaînes carbonées saturées. On dit aussi squelette carboné saturé.
Formule brute : Indique le nombre d'atomes de chaque élément sans préciser la structure.
Exemple : Éthanol C2H6O
Formule semi-développée : Représente les liaisons entre les atomes de carbone et les groupes fonctionnels-OH est le groupe hydroxyle, caractéristique de la fonction alcool (s'il y en a).
Exemple : Éthanol CH3-CH2-OH
Les entités organiques contiennent majoritairement des atomes de carbone et d'hydrogène.
Définition
Dans un alcane, il n'y a que des atomes de carbone C et d'hydrogène H.
La formule d'un alcane non cyclique est de la forme CnH2n+2.
La nomenclature des alcanes sert de base à celle de l'ensemble des molécules au squelette carboné saturé.
Le suffixe d'un alcane est -ane.
Nomenclature des alcanes à chaîne linéaire
Méthode :
Le radical (racine) dépend du nombre d'atomes de carbone :
1. méth-
2. éth-
3. prop-
4. but-
5. pent-
6. hex-
7. hept-
8. oct-
9. non-
Nomenclature des alcanes à chaîne ramifiée
Méthode :
1. ─ Le radical correspond à la chaîne principale (la plus longue).
2. ─ Une ramification est un groupe alkyleces groupes ne sont pas considérés comme des groupes fonctionnels, nommé en remplaçant -ane par -yle.
3. ─ On numérote la chaîne principale. Le sens choisi donne le numéro le plus petit possible au premier alkyle.
4. ─ On nomme la molécule. Préfixedonne les places + noms des alkyles, par ordre alphabétique + Radical + Suffixe ane.
Exercice : Écrire la formule semi-développée du méthylpropane.
─ Il y en a 3 à connaître (pour 4 familles fonctionnelles) :
1. carbonyle -CO (aldéhydes et cétones) ;
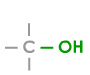
2. hydroxyle -OH (alcools) ;
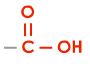
3. carboxyle -COOH (acide carboxylique).
Nomenclature
RADICAL
─ Le radical sera donné par la chaîne carbonée la + longue contenant le groupe caractéristique.
─ Cette chaîne est numérotée pour donner au groupe caractéristique la plus petite position.
PRÉFIXE
─ Un éventuel préfixedonne les places + noms des alkyles, par ordre alphabétique précède le radical.
SUFFIXE
─ Le suffixe-al, n-one, n-ol ou
-oïque pour les acides remplace le -e de l'alcane correspondant, précédé de sa place n dans la chaîne pour les cétones et les alcools.
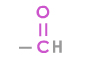
─ Si le groupe carbonyle est en bout de chaîne, c'est un aldéhyde (-al). Sinon, c'est une cétone (n-one).
RÉSUMÉ
| famille fonctionnelle | aldéhyde | cétone | alcool | acide carboxylique |
| groupe caractéristique | carbonyle | hydroxyle | carboxyle | |
 |
 |
 |
 |
|
| suffixe | -al | -n-one | -n-ol | acide ...oïque |
EXEMPLES ↓
La spectroscopie infrarouge (IR) permet d'identifier la famille fonctionnelle d'une molécule.
Elle ne permet pas d'identifier la structure complète de la molécule, seulement ses groupes caractéristiques.
Chaque liaison chimique vibre à une fréquence qui lui est propre. Lorsque la fréquence de l'infrarouge correspond à celle de la liaison, son énergie est absorbée.
Le spectre est la représentation de la transmittance \( \displaystyle\mathsf{\mathsfit {T} = \frac{\mathsfit {I}}{\mathsfit {I_0}}}\) (en %) en fonction du nombre d'onde \( \displaystyle\mathsf{\mathsfit {σ} = \frac{\mathsfit {1}}{\mathsfit {λ}}}\), en cm-1).
Spectre IR n°1

Spectre IR n°2
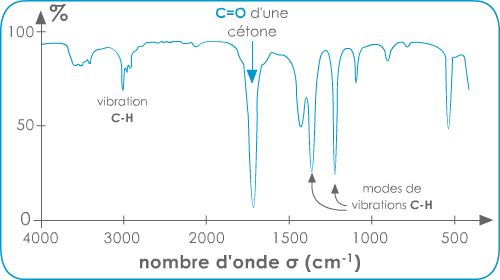
Interprétation. Spectre 1 : acide carboxylique. Le 2 : cétone.
Aux examens, les valeurs de la table du doc 1 vous seront données. 😊
doc 1 : Table IR
| liaison | σ (cm-1) | largeur | intensité |
| C-C |
|
faible | |
| C-H | 2850 3000 |
variable | moyen+ |
| C-H | 1260 1380 |
fines | fortes |
O-H alcool |
3200 3600 |
large | forte |
O-H carboxyle |
2500 3500 |
large | moyen+ |
C=O carboxyle |
1660 1740 |
fine | forte |
C=O aldéhyde |
1650 1740 |
fine | forte |
C=O cétone |
1700 1730 |
fine | forte |