Un atome est constitué d'un noyau chargé positivement et d'un nuageon dit aussi cortège électronique d'électrons chargés négativement.
1.1. Les constituants de l'atome
Les composants du noyau sont les nucléons. Les nucléons sont les protons et les neutrons
| proton | neutron | |
| charge | +e = 1,60.10-19 C | 0 |
| masse | 1,67.10-27 kg | 1,67.10-27 kg |
- La charge électrique q = + e du proton s'exprime en coulomb (C)
- Neutron est le nom donné aux nucléons neutres
- Proton et neutron ont des masses très procheselles seront égales dans les exercices.
Les électrons se déplacent autour du noyau.
| électron | |
| charge | - e = -1,6.10-19 C |
| masse | 9,1.10-31 kg |
1.2. Notation symbolique du noyau
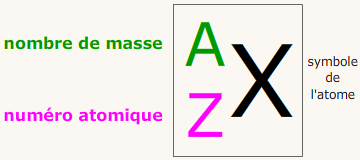
A : nombre total de nucléons
Z : nombre de protons → q =+Ze
Pour trouver le nombre de neutrons, on fait :
N = A - Z

2.1. Électroneutralité de l'atome
2.2. Masse de l'atome
Comparons les masses d'un nucléon et d'un électron :
\( \displaystyle\mathsf {\frac{1,67 \times 10^{-27}}{9,1 \times 10^{-31}}\ =\ {1,8 \times 10^3}} \)
La masse des électrons peut être considérée comme négligeable devant celle des nucléons.
La masse d'un atome est sensiblement égale à celle de son noyau.
matome = A.mnucléon
Application : Le noyau de l'atome d'or s'écrit \( \displaystyle\mathsf {^{197}_{\ 79}Au} \).
Donnée masse d'un nucléon = 1,67.10-27 kg
1. Que vaut A pour cet atome ? A est le nombre de nucléons.
2. Calculer la masse d'un atome d'or.
2.3. Taille d'un atome
Tous les atomes n'ont pas la même taille. On peut évoquer les ordres de grandeur :
- diamètre d’un atome : D =10–10 m
- diamètre d’un du noyau : d = 10–15 m
Comparons les tailles de l'atome et du noyau :
\( \displaystyle\mathsf {\frac{D}{d}\ =\frac{10^{-10}}{10^{-15}}\ =\ 100\ 000 \ =\ 10^5} \)
Application : Si l'atome est comparé à un terrain de foot, avec D = 100 m, le diamètre du noyau correspondra à celui
a) d'une tête d'épingle (d = 1 mm) ?
b) du point central (d = 20 cm) ?
c) du rond central (d = 18,3 m) ?