
\( \displaystyle\mathsf {^{A}_{Z}X} \) : Dans ce symbole , A est le nombre total de nucléons et Z le nombre des seuls protons.
Z, numéro atomique, donne son nom à l'élément, et réciproquement.
Il y a une bijectiontout élément de l'un ou l'autre des ensembles a une image et une seule dans l'autre entre l'ensemble des Z et celui des noms (ou symboles)
Exemple : Z = 6 suffit a identifier le carbone. Réciproquement, évoquer le carbone annonce Z = 6
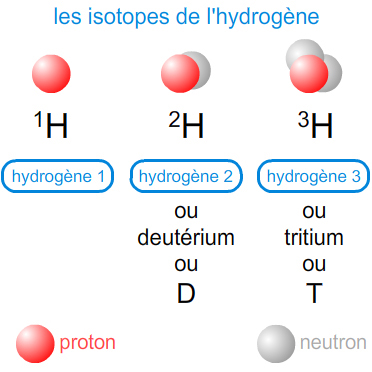
Les isotopes ont le même numéro atomique Z mais des nombres de masse A différents.
Les isotopes ont donc des nombres de neutrons différents.
Les isotopes ont le même nom. On les différencie en précisant leur nombre de masse.
Exemples : \( \displaystyle\mathsf {^{12}_{\ \ 6}C} \), \( \displaystyle\mathsf {^{13}_{\ \ 6}C} \) et \( \displaystyle\mathsf {^{14}_{\ \ 6}C} \) aussi notés \( \displaystyle\mathsf {^{12}_{}C} \), \( \displaystyle\mathsf {^{13}_{}C} \) et \( \displaystyle\mathsf {^{14}_{}C} \) puisque le symbole et le numéro atomique sont liés.
Règle de conservation :
Lors d'une transformation nucléaire il y a conservation de la somme des nombres de masse A et du nombre total de charges électriques Z.
2.1. Radioactivité
N'apparaît pas dans le programme de 2e →
Nucléaire : adj. relatif au noyau
Les réactions nucléaires s'écrivent avec les symboles :
- les noyaux : \( \displaystyle\mathsf {^{A}_{Z}X} \)
- le neutron : \( \displaystyle\mathsf {^{1}_{0}n} \)
- le proton : \( \displaystyle\mathsf {^{1}_{1}H} \) (ou \( \displaystyle\mathsf {^{1}_{1}p} \))
- l'électron : \( \displaystyle\mathsf {^{\ \ \ 0}_{-1}e} \)
- le positon : \( \displaystyle\mathsf {^{\ \ \ 0}_{+1}e} \)
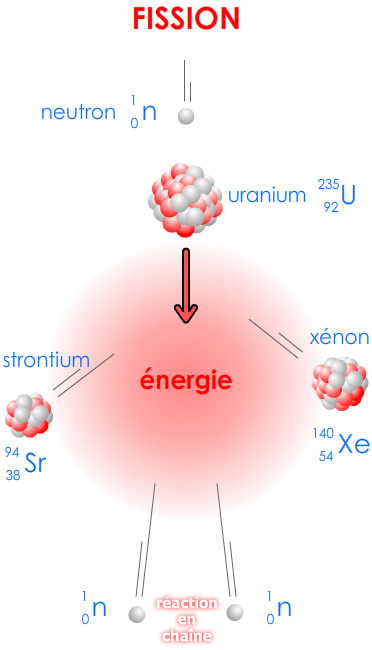
2.2. Fission
Les noyaux fissilesse dit d'un noyau qui peut subir une fission se trouvent parmi les noyaux lourds.
On parle de fission nucléaire quand un noyau très lourd se scinde en deux de taille moyenne
Exemple :
\( \displaystyle\mathsf {^{235}_{\ \ 92}U\ +\ ^{1}_{0}n\ →\ ^{94}_{38}Sr\ +\ ^{140}_{\ \ 54}Xe\ +\color{red} 2\ ^{1}_{0}n} \)
Remarque : l'uranium 235, l'uranium 238 et le plutonium 239 sont les noyaux fissiles les plus utilisés comme combustibles dans les centrales.
Ne retenez pas les noms des produits de fission, qui sont multiples. Retenez que 2 ou 3 neutrons sont émis à chaque fission, participant à la réaction en chaîne.
Exercice 1 : Compléter l'équation avec le nombre et le symbole des particules émises.
\( \displaystyle\mathsf {^{239}_{\ \ 94}Pu\ +\ ^{1}_{0}n\ →\ ^{135}_{\ \ 52}Te\ +\ ^{102}_{\ \ 42}Mo\ +\color{red} \ ...} \)
Indice : Utiliser la règle de conservation.
Exercice 2 : Compléter l'équation avec le symbole du produit de fission manquant.
\( \displaystyle\mathsf {^{235}_{\ \ 92}U\ +\ ^{1}_{0}n\ →{\color{red} ^{A}_{Z}X}\ +\ ^{138}_{\ \ 52}Te\ +\ 3\ ^{1}_{0}n} \)
Indice : Utiliser la règle de conservation.
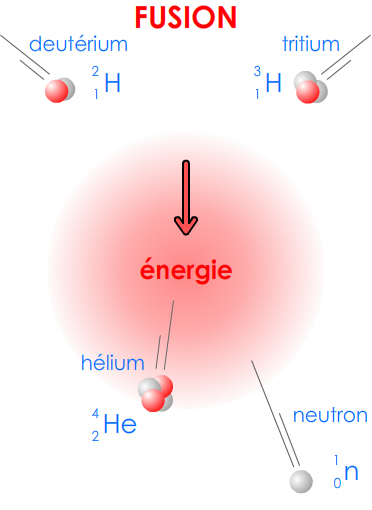
2.3. Fusion
Il y a fusion nucléaire lorsque deux noyaux légers s'unissent pour en former un seul, moins léger
Exemple :
\( \displaystyle\mathsf {^{2}_{1}H\ +\ ^{3}_{1}H\ →\ ^{4}_{2}He\ +\ ^{1}_{0}n} \)
C'est la réaction qui se produit dans le tokamakdispositif de confinement magnétique destiné à héberger et contrôler des réactions de fusion nucléaire du projet mondial ITER.
Dans les réacteurs nucléaires, les fissions libèrent de l'énergie qui chauffe l'eau d'un circuit primaire. L'eau du circuit secondaire passe à l'état de vapeur pour actionner mécaniquement une turbine, entraînant un alternateur.
Dans le Soleil, les fusions libèrent de l'énergie qui traverse l'espace par rayonnement.
Les réactions nucléaires sont exothermiques.
PHYSIQUE
L'état peut être modifié (s, l ou g), la température, la pression... mais les molécules sont les mêmes avant et après.
\( \displaystyle\mathsf {H_{2}O_{(s)}\ →\ H_{2}O_{(l)}} \)
CHIMIQUE
Les cortèges électroniques sont modifiés, les liaisons, et donc les molécules... mais les noyaux sont les mêmes avant et après.
\( \displaystyle\mathsf {C\ +\ O_{2}\ →\ CO_{2}} \)
NUCLÉAIRE
Pour la désintégration α, β, la fission et la fusion, les noyaux sont différents. Les éléments ne sont pas les mêmes avant et après.
\( \displaystyle\mathsf {^{235}_{\ \ 92}U\ +\ ^{1}_{0}n\ →\ ^{94}_{38}Sr\ +\ ^{140}_{\ \ 54}Xe\ +\ 2\ ^{1}_{0}n} \)